
AmBeed文献解读|Nature Communications
支链内体干扰物 (BEND) 脂质介导 mRNA 和 CRISPR-Cas9 核糖核蛋白复合物的递送,用于肝脏基因编辑和 T 细胞工程

2025年1月24日,宾夕法尼亚大学Michael J. Mitchell研究团队发表题为《Branched endosomal disruptor (BEND) lipids mediate delivery of mRNA and CRISPR-Cas9 ribonucleoprotein complex for hepatic gene editing and T cell engineering》的研究。文章的核心内容是关于一种新型的脂质纳米颗粒(Lipid Nanoparticles, LNPs)——分支内质网破坏者(Branched Endosomal Disruptor, BEND)的研究。这些脂质被设计用于提高mRNA和CRISPR-Cas9核糖核蛋白复合物的递送效率,特别是在肝脏基因编辑和T细胞工程中的应用。
背景知识
· mRNA治疗作为一种有潜力的临床方式,具有能够编码任何蛋白质、较低剂量需求以及不会整合到基因组中的优点。然而,mRNA在临床应用中的成功受到递送困难的限制,因为它在血液中迅速降解,无法自行穿过细胞膜,并且可能引发不必要的免疫反应。
· 脂质纳米颗粒(LNPs)是目前最先进的非病毒药物载体,用于核酸递送。LNPs通过包裹mRNA,保护其免受降解和免疫识别,并帮助引导mRNA到达特定位置。LNPs的关键成分是离子化脂质(Ionizable Lipid, IL),它在mRNA封装和细胞摄取中起着重要作用。
研究方法
· 研究团队开发了一种合成平台,用于生成具有末端分支结构的离子化脂质。这些脂质通过在脂质链末端添加分支基团,增加了肝脏mRNA和RNP复合体的传递效率以及基因编辑效率。
· 通过一系列实验,研究团队确定了这种脂质结构能够诱导的内质网穿透和破坏效果更显著,从而提高mRNA的传递效率。
· 研究中使用了多种实验方法,包括LNPs的合成、mRNA和RNP复合体的封装、细胞实验、动物模型实验以及分子动力学模拟等,以验证BEND脂质的效果和机制。
AmBeed产品
1,12-dibromododecane(A111960)
1,12-dibromododecane主要用作有机合成中间体,可用于合成多种有机化合物,例如在医药、农药等领域作为中间体。
在此篇文献中,通过与钾叔丁氧基钾(简称KOtBu,化学式为KOC(CH₃)₃)反应,1,12-dibromododecane 被转化为12-溴十二烯。这一反应利用了E2消除反应机制,生成了含有12个碳原子的溴代烯烃。这种溴代烯烃随后被用于与不同的Grignard试剂反应,生成具有末端分支结构的烯烃(alkenes),这些烯烃是合成BEND脂质的关键中间体。
N1-(2-(4-(2-aminoethyl)piperazin-1-yl)ethyl)ethane-1,2-diamine(A505336)
N1-(2-(4-(2-aminoethyl)piperazin-1-yl)ethyl)ethane-1,2-diamine是一种哌嗪类化合物,常用于药物合成和生物化学研究,作为重要的中间体。它具有较高的生物活性和合成潜力,可用于制备脂质纳米颗粒等前沿生物材料。
在此篇文献中,该产品用于合成BEND脂质,其作为胺基核心(amine core),与合成的末端分支环氧烷(epoxides)反应,生成具有不同分支结构的离子化脂质(ILs)。这些脂质随后被用于构建脂质纳米颗粒(LNPs),用于封装mRNA和CRISPR-Cas9核糖核蛋白复合体(RNP)。

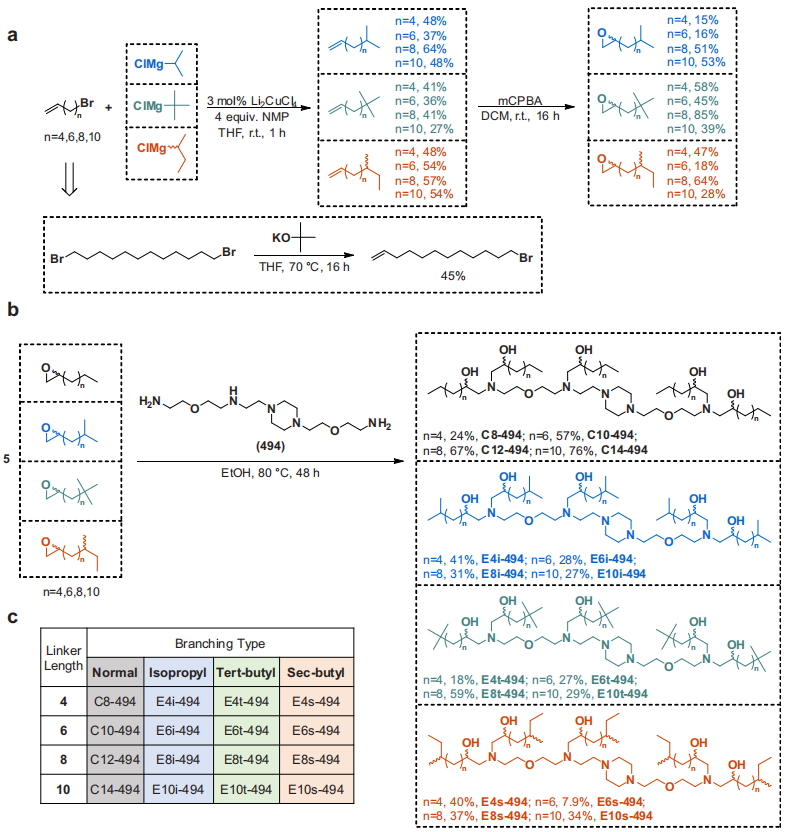
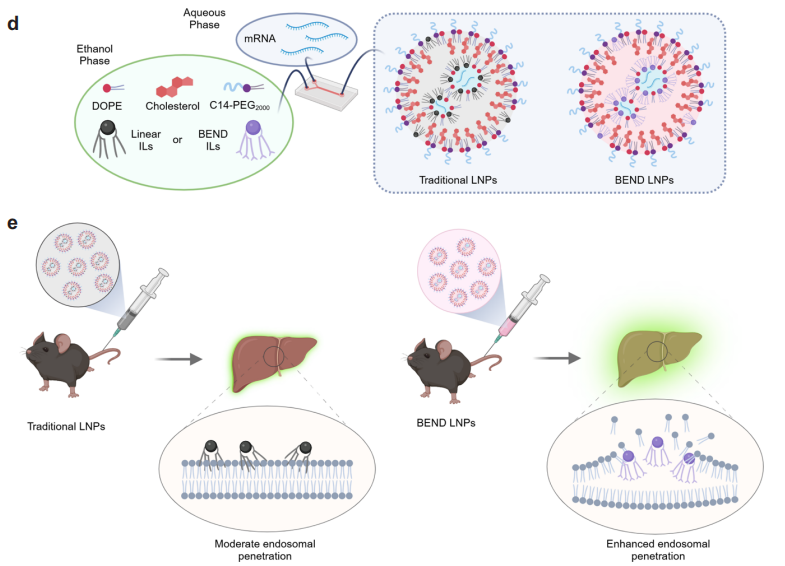
图1. 分支型内质网破坏剂(BEND)离子化脂质平台的合成方法
1,12-dibromododecane(购买自AmBeed)通过E2消除反应合成具有特定长度的溴代烯烃,溴代烯烃通过铜催化的C-C偶联反应与支链Grignard试剂结合生成支链烯烃,随后经mCPBA氧化生成支链环氧化物,再与多胺核心(如494或200)通过SN2反应合成BEND脂质。该合成方法模块化、高效,可在3天内完成16种不同结构的脂质合成,并验证了其用于脂质纳米颗粒(LNPs)的可行性。支链结构设计旨在增强内体逃逸,促进mRNA和蛋白质的递送。
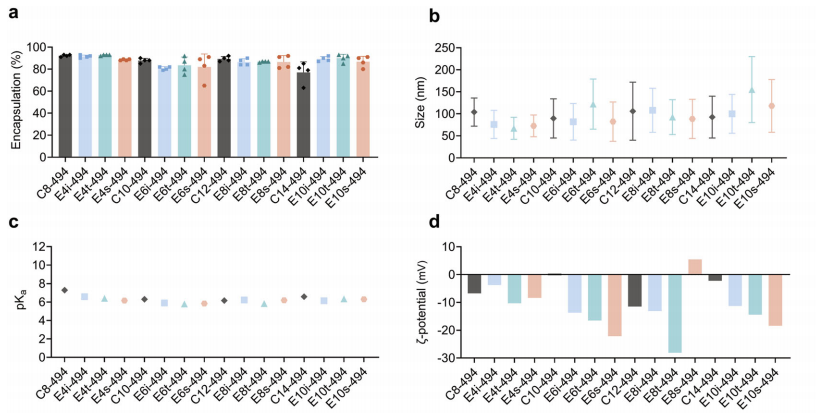

图2. BEND 494核脂质纳米颗粒(LNPs)在肝脏mRNA转染方面优于线性494核LNPs
与线性脂质相比,BEND脂质显著提高了小鼠肝脏中荧光素酶mRNA的表达(如E4t-494的肝脏总通量比C12-200高1.5倍)。所有BEND LNPs均表现出>80%的封装率和中性表面电荷(ζ电位),且粒径分布均匀(70-160 nm)。结果表明,支链结构通过增强内体逃逸而非理化特性差异来提升递送效率。

图3. BEND 200核脂质纳米颗粒(LNPs)增强了mRNA递送和Cas9介导的基因编辑
使用200核心(N1-(2-(4-(2-aminoethyl)piperazin-1-yl)ethyl)ethane-1,2-diamine,购买自AmBeed)与不同长度和不同分支类型的环氧烷反应,合成了六种BEND脂质:E8i-200、E8t-200、E8s-200、E12i-200、E12t-200、E12s-200。以及作为对照,合成了两种线性脂质:C8-200和C12-200。实验表明,BEND脂质(如E4s-200)显著降低小鼠血清中的转甲状腺素蛋白(TTR)水平(90%敲低),并诱导更高的基因插入/缺失(indel)效率(60-70%),优于线性脂质C12-200(55%)。此外,BEND脂质减少了肝脏毒性标志物(AST/ALT),验证了其高效性与安全性并存的特点。

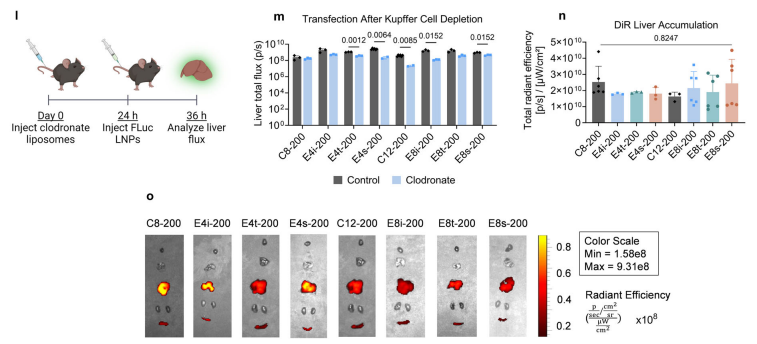
图4. BEND和线性脂质纳米颗粒(LNPs)在理化特性、蛋白冠形成以及体内肝脏积累方面表现出相似性
BEND与线性脂质的LNPs在粒径、PDI、ζ电位和稳定性(PBS/DMEM中)上无显著差异,表明其结构变化对整体形态影响较小。ApoE(载脂蛋白E)敲除小鼠实验表明,BEND LNPs依赖ApoE介导的肝靶向机制。此外,巨噬细胞清除实验显示,除C8-200外,BEND LNPs的肝脏转染依赖库普弗细胞,但支链结构本身不影响器官积累(DIR荧光实验)。

图5. BEND离子化脂质(ILs)通过增强内质网破坏来提高脂质纳米颗粒(LNPs)的递送效率
BEND脂质的LNPs在内质网破坏能力上显著高于线性脂质的LNPs。分子动力学模拟进一步揭示了BEND脂质能够更深入地插入脂质双层,从而更有效地破坏内质网膜。这些发现为BEND脂质在基因治疗和mRNA药物传递中提供了重要的理论支持。
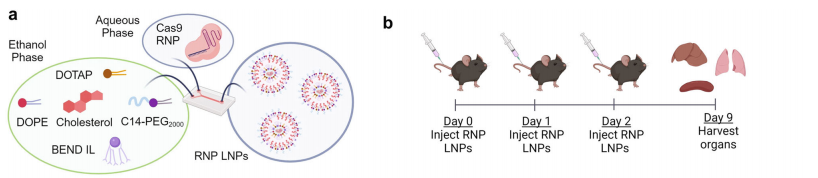


图6. BEND离子化脂质(ILs)能够实现模块化的CRISPR-Cas9核糖核蛋白复合物基因编辑
BEND脂质LNPs在肝脏中显示出更高的基因编辑效率和更好的靶向性,同时在不同细胞类型中表现出细胞类型特异性的编辑效率。这些发现为BEND脂质在基因治疗中的应用提供了重要的实验依据。
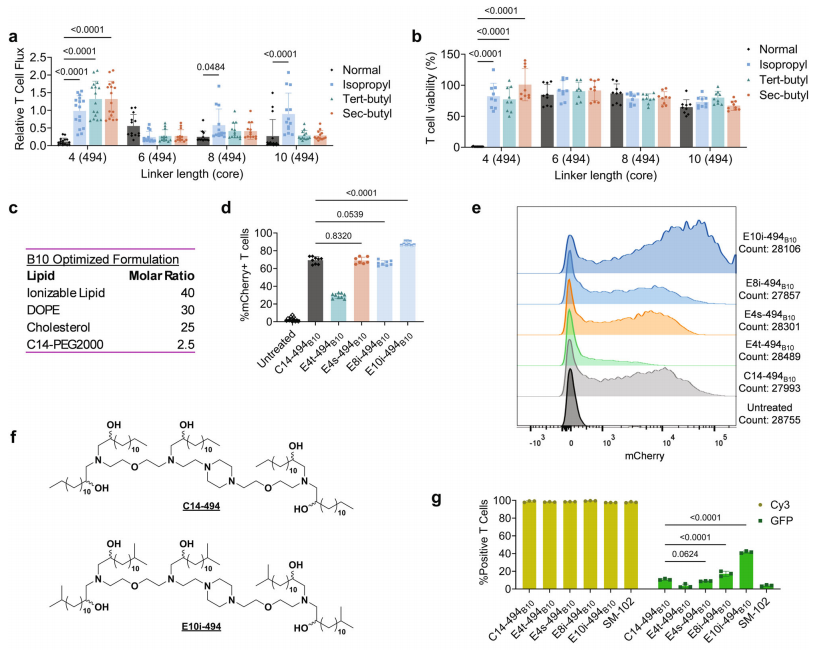

图7. BEND脂质纳米颗粒通过内质网逃逸介导T细胞转染
研究发现,BEND脂质的LNPs在T细胞转染中表现出更高的效率和更低的毒性,特别是E4t-494、E4s-494和E10i-494等脂质。通过优化配方,这些LNPs能够转染超过80%的T细胞,显示出显著的转染能力。此外,通过流式细胞术和共聚焦显微镜成像,研究进一步揭示了BEND脂质通过增强内质网逃逸能力来提高mRNA传递效率的机制,表明其在T细胞工程和基因治疗中的潜在应用价值。
研究结论
· BEND脂质通过其独特的结构设计,显著提高了LNPs在mRNA传递和基因编辑中的效率,特别是在肝脏和T细胞中的应用。
· BEND脂质的末端分支结构能够增强内质网逃逸能力,从而提高mRNA和蛋白质的传递效率。
· 这些发现为未来的基因治疗和mRNA药物递送提供了新的策略和工具,具有重要的临床应用前景。
Doi: https://doi.org/10.1038/s41467-024-55137-6

















